BS Bùi Thế Dũng*, BS Lương Cao Sơn*, BS Đoàn Thái**
TÓM TẮT
Mục tiêu: Đánh giá tính hiệu quả và an toàn của cắt đốt bằng sóng cao tần qua catheter ở bệnh nhân có hội chứng Wolff-Parkinson-White hoặc cơn nhịp nhanh kịch phát trên thất liên quan đến đường dẫn truyền phụ ẩn nhĩ thất.
Phương pháp và kết quả: Mô tả hàng loạt ca. Trong 28 tháng (từ tháng 1/2008 đến tháng 5/2010), có 160 bệnh nhân đã được thăm dò điện sinh lý và cắt đốt đường dẫn truyền phụ nhĩ thất để điều trị hội chứng Wolff-Parkinson-White hoặc cơn nhịp nhanh kịch phát trên thất liên quan đến đường dẫn truyền phụ ẩn nhĩ thất. Tất cả bệnh nhân đều được tiến hành cắt đốt trong lần thăm dò điện sinh lý đầu tiên. Thời gian thủ thuật và thời gian soi tia X được ghi lại ở mỗi bệnh nhân. Kết quả: 83 trường hợp đường dẫn truyền phụ hiện và 77 trường hợp là ẩn. 93 trường hợp đường dẫn truyền phụ nằm ở thành tự do thất trái, 28 trường hợp ở thành tự do thất phải, 24 trường hợp ở vùng sau vách (3 trường hợp nằm ở thượng tâm mạc phải cắt đốt trong xoang vành), 10 trường hợp ở thành trước, 3 trường hợp ở trước vách phải, 2 trường hợp ở giữa vách phải. 152 trường hợp (95%) được cắt đốt thành công. 4 trường hợp tái phát và được cắt đốt thành công lần 2. Thời gian thủ thuật trung bình là 93 ± 39 phút, dài nhất là 240 phút ở bệnh nhân có nhiều đường dẫn truyền phụ và ngắn nhất là 30 phút ở bệnh nhân có đường dẫn truyền phụ vùng giữa vách. Thời gian chiếu tia X trung bình là 16 ± 12 phút. Tai biến thủ thuật quan trọng chỉ gặp ở 1 trường hợp.
Kết luận: Kết quả nghiên cứu một lần nữa cho thấy cắt đốt bằng sóng cao tần đường dẫn truyền phụ nhĩ thất có thể được thực hiện hiệu quả, an toàn và nhanh chóng ở đa số bệnh nhân, mà không cần phải dùng thuốc điều trị kéo dài.
ABSTRACT
radiofrequency catheter ablation of accessory ATRIOVENTRICULAR PATHWAYS: RESULTS IN 160 CONSECUTIVE PATIENTS
Bui The Dung M.D*, Luong Cao Son*, Doan Thai**
Objective: The purpose of this study was to evaluate the efficacy and safety of radiofrequency catheter ablation of accessory atrioventricular (AV) pathways with Wolff-Parkinson-White syndrome or paroxysmal supraventricular tachycardia involving a concealed accessory AV pathways.
Methods and results: Case series study. One hundred sixty consecutive patients with the Wolff-Parkinson-White syndrome or paroxysmal supraventricular tachycardia involving a concealed accessory AV pathways underwent electrophysiology study and catheter ablation with the use of radiofrequency current during 28 months (from Jan 2008 to May 2010). In all patients, catheter ablation was performed at the time of an initial electrophysiology test. The time of total procedure was recorded for each patient, as was the total duration of fluoroscopy. Eighty-three accessory pathways (APs) were manifest and 77 were concealed. Ninety-three were located in the free wall of the left ventricle, 28 were in the right free wall, 24 were posteroseptal (3 were epicardial APs ablated via coronary sinus), 10 were anterior, 3 were anteroseptal, and 2 were mid-septal. One hundred fifty-two (95%) patients had all accessory AV connections successfully ablated. For cases recurred and were ablated successfully in the 2nd procedures. Mean duration of the entire procedure was 93 ± 39 minutes. Procedure duration was longest in patients with multiple APs (240 minutes), shortest in patients with mid-septal APs (30 minutes). Mean fluoroscopic time was 16 ± 12 minutes. A major complication occurred in only 1 patient (0.6%).
Conclusion: The results of this study indicate that catheter ablation of APs with radiofrequency current can be performed efficaciously, safely and expeditiously in a majority of patients. This therapeutic approach avoids the need for long-term antiarrhythmic drug therapy in the majority of patients with the Wolff-Parkinson-White syndrome or with symptomatic tachycardias involving accessory pathways.
-------------------------
(*) Bệnh viện Đại học Y Dược
(**) Bệnh viện FV
ĐẶT VẤN ĐỀ
Điều trị cổ điển hội chứng Wolff-Parkinson-White (HC WPW) thường là bằng thuốc chống loạn nhịp. Gần đây, cắt đốt qua catheter đường dẫn truyền phụ nhĩ thất đã được chứng minh có tỷ lệ thành công rất cao (gần 100%).
Mục tiêu của nghiên cứu này là báo cáo kết quả và biến chứng của cắt đốt bằng sóng cao tần đường dẫn truyền phụ nhĩ thất (cầu Kent) qua 160 trường hợp tại Bệnh viện Đại học Y Dược, Thành phố Hồ Chí Minh.
PHƯƠNG PHÁP NGHIÊN CỨU
Đối tượng nghiên cứu là 160 bệnh nhân nhập viện BV ĐHYD từ tháng 1/2008 đến tháng 5/2010 để được điều trị HC WPW hoặc cơn nhịp nhanh kịch phát trên thất liên quan đến đường dẫn truyền phụ nhĩ thất. Tuổi trung bình là 41 ± 14 tuổi, BN nhỏ tuổi nhất là 11 tuổi và lớn tuổi nhất là 73 tuổi.
Thăm dò điện sinh lý:
Tất cả bệnh nhân được nhịn ăn trước thủ thuật ít nhất 6 giờ, ngưng tất cả các thuốc chống loạn nhịp trước thủ thuật ít nhất 5 ngày và được cam kết đồng ý làm thủ thuật trước. Hai catheter (KT) 4 cực 5F được đưa qua tĩnh mạch đùi phải vào thất phải và bó His, một KT 4 cực 5F hoặc 10 cực 6F có thể uốn cong ở đầu được đưa vào xoang vành qua đường tĩnh mạch đùi phải. Tiến hành kích thích thất và nhĩ theo chương trình để tạo cơn nhịp nhanh và đo đạc các thông số cần thiết với máy UVH 3000 của hãng Biotronik.
Quy trình cắt đốt:
Sau khi định vị đường dẫn truyền phụ, vị trí chính xác cần đốt được “dò tìm “ (mapping) trên vòng van 2 lá và 3 lá bởi một catheter cắt đốt 7F 4 cực có thể uốn cong ở đầu. Điện đồ lưỡng cực từ hai cực xa của catheter cắt đốt được lọc ở tần số 50-500 Hz, và ghi lại ở tốc độ 100mm/giây.
Đường dẫn truyền phụ bên trái được tiếp cận bằng cách đưa catheter cắt đốt vào động mạch đùi phải và đi ngược qua van động mạch chủ vào thất trái, rồi dò tìm vị trí chính xác của đường dẫn truyền phụ từ mặt thất hoặc mặt nhĩ của vòng van 2 lá (Hình 1). Đường dẫn truyền phụ bên phải được tiếp cận bằng cách đưa catheter qua tĩnh mạch chủ dưới vào mặt nhĩ của vòng van 3 lá (Hình 2). Để cắt đốt đường dẫn truyền phụ vùng sau vách, catheter cắt đốt được đưa vào qua tĩnh mạch chủ dưới để dò tìm trên vòng van 3 lá và lỗ đổ vào nhĩ phải của xoang vành. Khi cắt đốt vùng sau vách bên phải không thành công, catheter cắt đốt được đưa vào thất trái để dò tìm trên vòng van 2 lá vùng sau vách. Nếu cắt đốt cả 2 bên trái và phải không thành công, catheter sẽ được đưa vào dò tìm trong các nhánh của xoang vành.
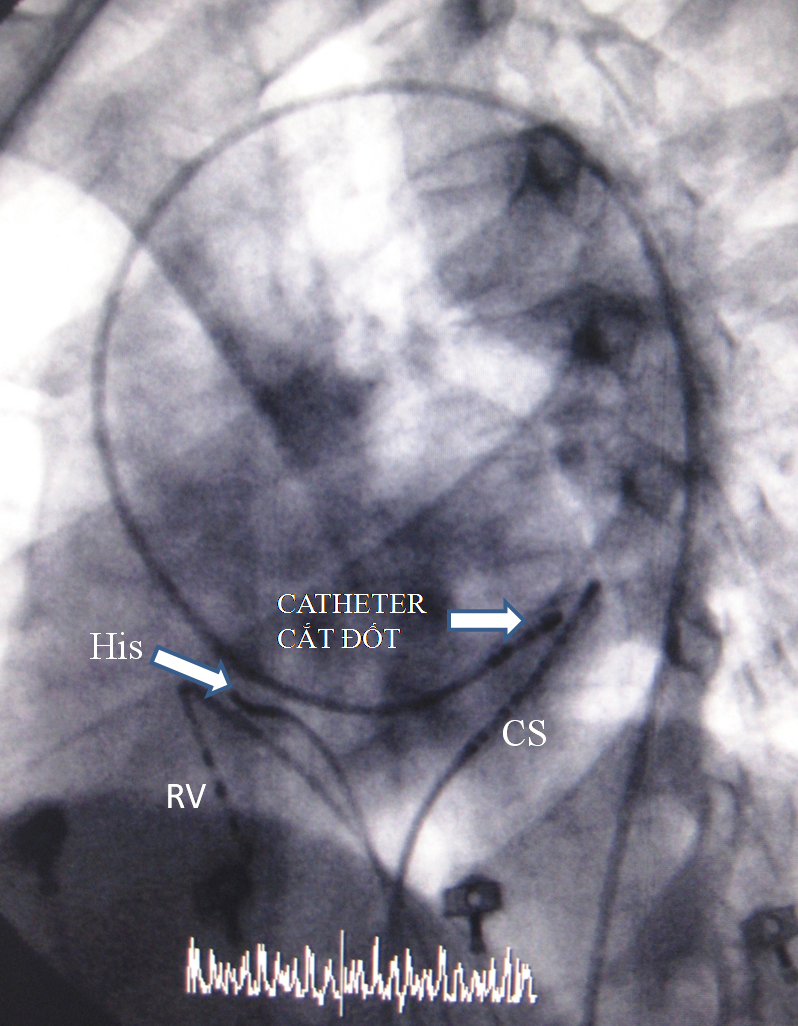
Hình 1: Hình ảnh X quang vị trí catheter cắt đốt đường dẫn truyền phụ thành tự do bên trái (mặt phẳng chếch trước trái 600 ). RV:catheter thất phải, CS:catheter xoang vành, His: catheter bó His.
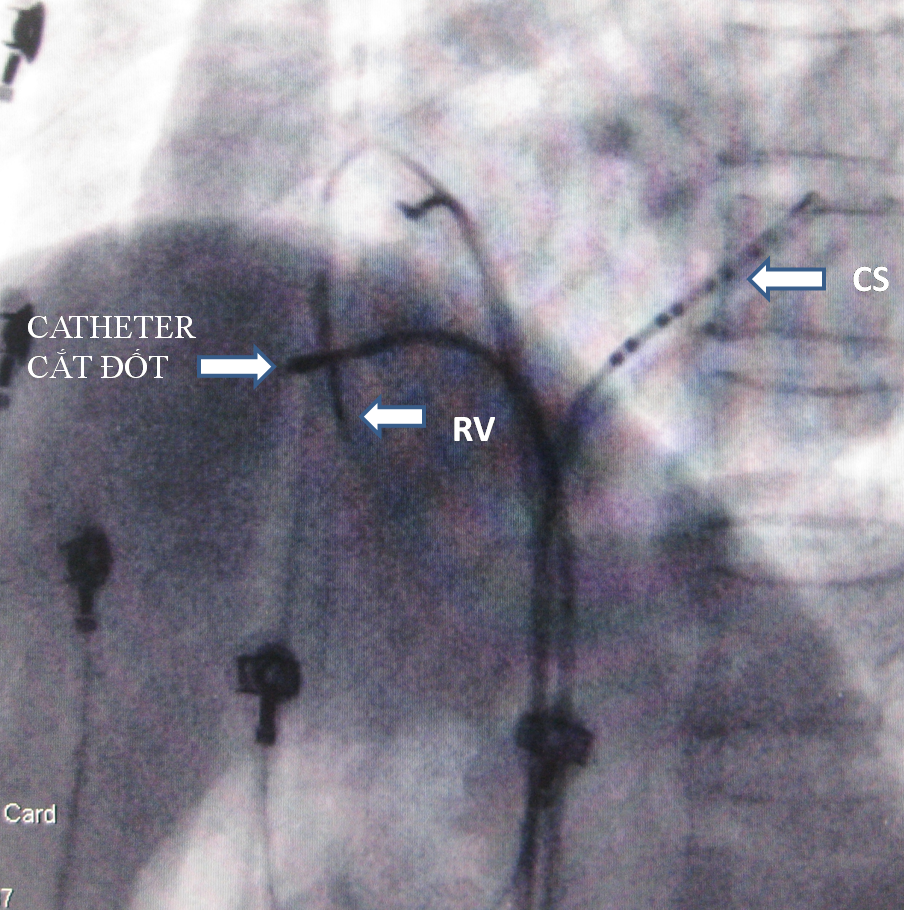 Hình 2: Hình ảnh X quang vị trí catheter cắt đốt đường dẫn truyền phụ thành tự do bên phải (mặt phẳng chếch trước trái 600 ). RV:catheter thất phải, CS:catheter xoang vành, His: catheter bó His.
Hình 2: Hình ảnh X quang vị trí catheter cắt đốt đường dẫn truyền phụ thành tự do bên phải (mặt phẳng chếch trước trái 600 ). RV:catheter thất phải, CS:catheter xoang vành, His: catheter bó His.
Đường dẫn truyền phụ nhĩ thất có dẫn truyền xuôi (HC WPW) sẽ được dò tìm trong nhịp xoang hoặc tạo nhịp nhĩ liên tục. Vị trí được chọn để cắt đốt khi ghi nhận sóng khử cực thất sớm hơn sóng delta của ECG bề mặt, có sự pha trộn giữa sóng nhĩ và sóng thất và là sóng hoàn toàn âm trên catheter cắt đốt đơn cực (RF uni) (Hình 3) Đường dẫn truyền phụ ẩn được dò tìm trong cơn nhịp nhanh hoặc khi tạo nhịp thất liên tục. Vị trí cắt đốt khi sóng nhĩ dẫn truyền ngược đến sớm nhất và âm tuyệt đối trên catheter cắt đốt đơn cực (3,4,8,13) (Hình 4).
Cắt đốt qua catheter dùng năng lượng có tần số radio được lọc ở 50-500 Hz, ghi ở tốc độ 100 mm/giây, máy đốt HAT 300 – OSYPKA.
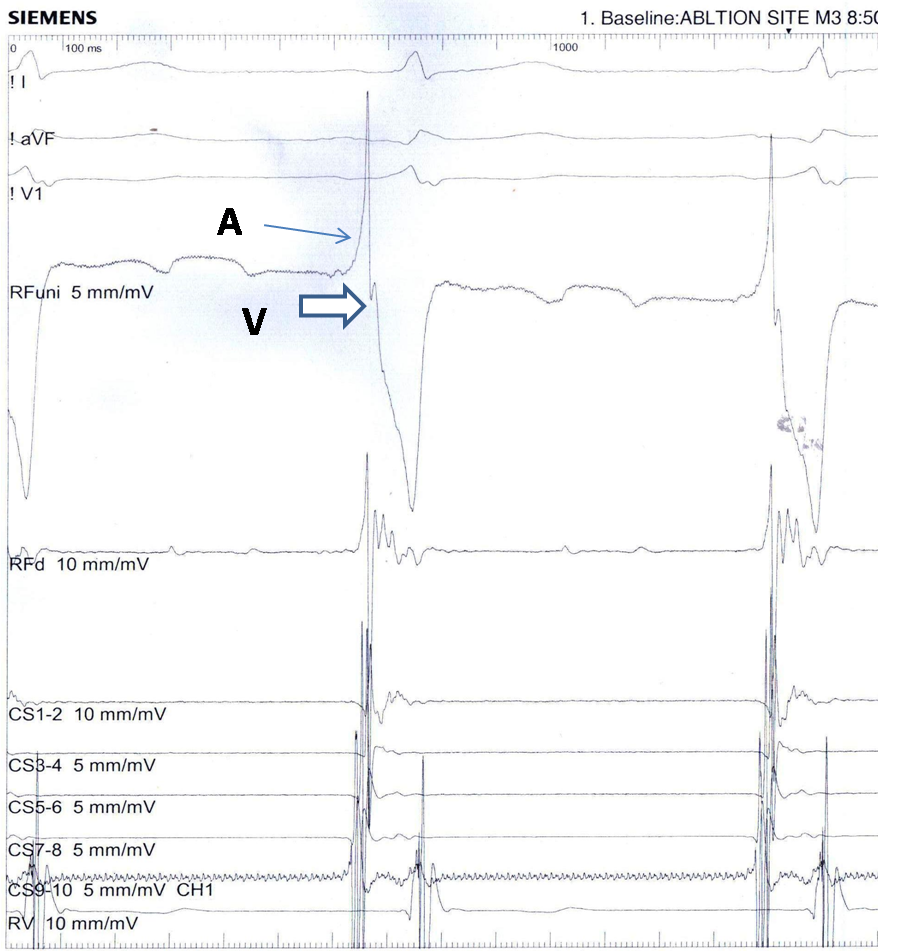 Hình 3: Cắt đốt đường dẫn truyền phụ thành tự do bên trái trong nhịp xoang. Điện thế tại catheter cắt đốt lưỡng cực (RFd) ghi nhận sự pha trộn (fusion) giữa sóng nhĩ (A) và sóng thất (V), tại catheter cắt đốt đơn cực (RFuni) nhận sóng thất gần như hoàn toàn âm, dốc đứng và đến sớm hơn sóng delta của ECG bề mặt.
Hình 3: Cắt đốt đường dẫn truyền phụ thành tự do bên trái trong nhịp xoang. Điện thế tại catheter cắt đốt lưỡng cực (RFd) ghi nhận sự pha trộn (fusion) giữa sóng nhĩ (A) và sóng thất (V), tại catheter cắt đốt đơn cực (RFuni) nhận sóng thất gần như hoàn toàn âm, dốc đứng và đến sớm hơn sóng delta của ECG bề mặt.
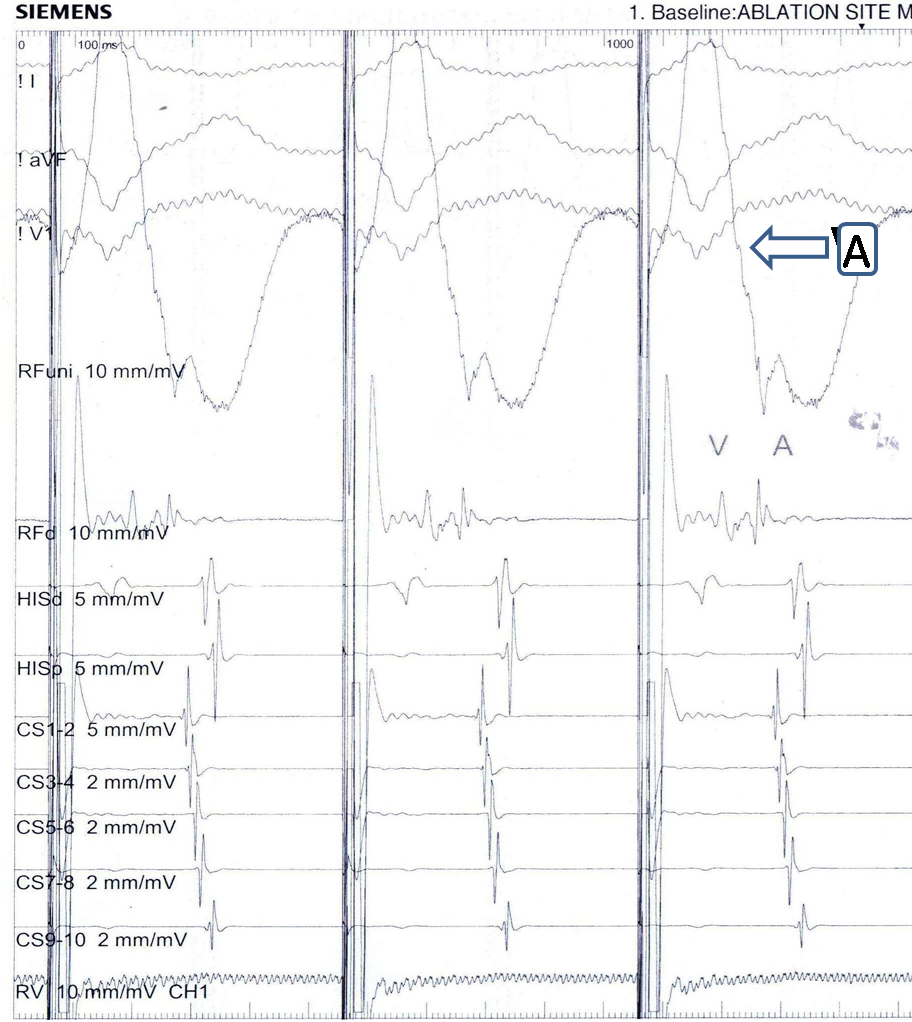 Hình 4: Cắt đốt đường dẫn truyền phụ thành tự do bên trái trong khi tạo nhịp thất liên tục. Điện thế tại catheter cắt đốt lưỡng cực (RFd) ghi nhận sự pha trộn (fusion) giữa sóng thất (V) và sóng nhĩ (A) tại catheter cắt đốt đơn cực (RFuni) nhận sóng nhĩ hoàn toàn âm, dốc đứng và đến sớm hơn sóng nhĩ trên catheter xoang vành (CS).
Hình 4: Cắt đốt đường dẫn truyền phụ thành tự do bên trái trong khi tạo nhịp thất liên tục. Điện thế tại catheter cắt đốt lưỡng cực (RFd) ghi nhận sự pha trộn (fusion) giữa sóng thất (V) và sóng nhĩ (A) tại catheter cắt đốt đơn cực (RFuni) nhận sóng nhĩ hoàn toàn âm, dốc đứng và đến sớm hơn sóng nhĩ trên catheter xoang vành (CS).
Theo dõi sau thủ thuật cắt đốt
Sau thủ thuật bệnh nhân (BN) được theo dõi dấu hiệu sinh tồn mỗi 6 giờ, đo lại ECG sau 24 giờ (lưu ý tìm có dấu kích thích sớm hay không).
BN tái khám sau ra viện một tháng và được đo lại ECG hoặc bất kỳ khi nào BN có triệu chứng như trước khi cắt đốt để được đo ECG đánh giá tái phát.
Phân tích thống kê
Dữ liệu được nhập và xử lý thống kê bằng phần mềm SPSS 17.0 for Windows.
KẾT QUẢ
Dữ liệu cơ bản
Trong nghiên cứu này có 160 bệnh nhân đã được thăm dò điện sinh lý và cắt đốt đường dẫn truyền phụ nhĩ thất để điều trị hội chứng WPW hoặc cơn nhịp nhanh kịch phát trên thất liên quan đến đường dẫn truyền phụ ẩn nhĩ thất. 80 BN là nữ và 80 BN là nam. 83 trường hợp đường dẫn truyền phụ hiện và 77 trường hợp là ẩn. Số lượng cầu Kent trung bình là 1±0,1 (nhiều nhất là 2 cầu Kent trên cùng 1 BN). 93 trường hợp đường dẫn truyền phụ nằm ở thành tự do bên trái (58,1%), 28 trường hợp ở thành tự do bên phải (17,5%), 24 trường hợp ở vùng sau vách (15,0%) trong đó có 3 trường hợp nằm ở thượng tâm mạc phải cắt đốt trong xoang vành, 3 trường hợp ở thành trước vách phải (1,9), 2 trường hợp ở giữa vách phải (1,2%) (Hình 5). Thời gian trơ trung bình của đường dẫn truyền nhĩ thất hiện là 275 ± 84 miligiây, và thời gian trơ trung bình dẫn truyền ngược của đường phụ ẩn là 278 ± 93 miligiây. Cơn nhịp nhanh vòng vào lại nhĩ thất thuận chiều tạo được ở 115 bệnh nhân và có độ dài chu kỳ nhịp nhanh trung bình là 322 ± 62 mili giây (tần số trung bình khoảng 182 lần/phút); rung nhĩ ghi nhận được ở 4 BN trong quá trình thăm dò và được chuyển nhịp bằng Amiodaron tiêm mạch.
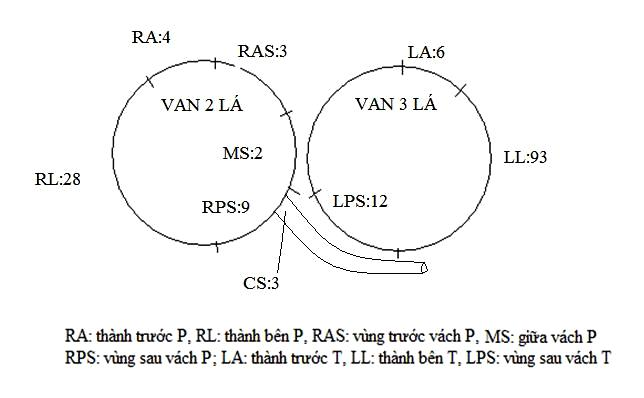 Hình 5: Vị trí và số lượng đường dẫn truyền phụ
Hình 5: Vị trí và số lượng đường dẫn truyền phụ
Kết quả cắt đốt
152 trường hợp cắt đốt thành công đường dẫn truyền phụ nhĩ thất (95%) và không còn triệu chứng trong suốt thời gian theo dõi từ 2 đến 28 tháng, trong đó có 1 trường hợp thất bại được cắt đốt thành công ở lần thủ thuật thứ hai. Có 4 trường hợp tái phát (2,5%) được cắt đốt lại thành công. Một trường hợp cầu Kent sau vách cắt đốt lần một qua đường nội mạc thất bại được cắt đốt thành công qua xoang vành ở lần thủ thuật thứ 2.
8 trường hợp cắt đốt thất bại (5%) gồm các vị trí: 2 thành tự do bên phải, 2 thành bên thất trái, 1 thành trước bên trái, 2 vùng giữa vách phải, 1 ở thành trước vách phải (Bảng 1).
Bảng 1: Kết quả cắt đốt theo vị trí đường dẫn truyền phụ
| Vị trí |
Số lượng |
Thành công |
Thất bại |
| Tự do bên (T) |
93 |
91 (97,8%) |
2 (2,2%) |
| Tự do bên (P) |
28 |
26 (92,8%) |
2 (7,2%) |
| Sau vách |
24 |
24 (100%) |
0 (0%) |
| Thành trước |
10 |
9 (90%) |
1 (10%) |
| Trước vách |
3 |
2 (66,7%) |
1 (3,3%) |
| Giữa vách |
2 |
0 (0%) |
2 (100) |
| Tổng cộng |
160 |
152 (95%) |
8 (5%) |
Thời gian thủ thuật
Thời gian thủ thuật tính từ lúc chọc mạch đến khi kết thúc thủ thuật (gồm 30 phút theo dõi cho mỗi trường hợp) trung bình là 93,7 ± 39 phút. Thời gian thủ thuật ngắn nhất là 30 phút ở BN có cầu Kent ở vị trí giữa vách bên phải (trường hợp thất bại). Thời gian thủ thuật dài nhất là 240 phút ở
bệnh nhân có 2 đường dẫn truyền phụ nằm ở thành tự do bên trái và cắt đốt thất bại (chỉ đốt được 1 đường dẫn truyền phụ).Thời gian chiếu tia X trung bình 16,7 ± 12,3 phút, ngắn nhất là 1 phút, dài nhất là 60 phút. Thời gian cầu Kent biến mất của nhát đốt thành công là 5,3 ± 2,9 giây. Số nhát đốt trung bình là 2,7 ± 2,6 (Bảng 2).
Bảng 2: Thời gian cắt đốt đường dẫn truyền phụ
| |
Số BN |
Tối thiểu |
Tối đa |
Trung bình |
Độ lệch chuẩn |
| Thời gian thủ thuật |
160 |
30 |
240 |
93.72 |
39.018 |
| Thời gian chiếu tia |
160 |
1 |
60 |
16.78 |
12.321 |
| Số nhát đốt |
160 |
1 |
15 |
2.74 |
2.695 |
| Thời gian Kent biến mất |
152 |
1 |
20 |
5.37 |
2.904 |
Biến chứng
Một BN xuất hiện tụ máu lớn tại chỗ chọc động mạch đùi phải sau thủ thuật cắt đốt đường dẫn truyền phụ vùng sau vách bên trái. Sau khi băng ép và bất động 24 giờ thì lại bị huyết khối tĩnh mạch chậu đùi bên trái.
BÀN LUẬN
Các dữ liệu chính
Vị trí đường dẫn truyền phụ: Bên trái chiếm ưu thế (69,4%) so với bên phải (30,6%).Tỷ lệ chi tiết thành tự do bên trái: 58,1%, thành tự do bên phải: 17,5%, vùng sau vách 15%. Vị trí ít gặp nhất là vùng giữa vách phải ít gặp nhất (1,2%) và trước vách phải (1,9%). Tỷ lệ này cũng tương tự như các thống kê của y văn (3,4,13).
95% của 160 trường hợp (152 BN) được cắt đốt thành công và không còn triệu chứng trong suốt thời gian theo dõi. Tỷ lệ này tương đương các báo cáo của Hugh Calkins (1,2), Fred Morady (8) , hơi thấp hơn so với tỷ lệ thành công của Jackman và Tôn Thất Minh (99%) (6,12). Vị trí có tỷ lệ cắt đốt thành công cao nhất là thành sau vách (100%) có lẽ là do chúng tôi cố gắng dò tìm trong các nhánh của xoang vành sau khi đã tiếp cận cả hai bên phải và trái vùng sau vách thất bại (có 3/160 trường hợp là đường dẫn truyền phụ thượng tâm mạc được cắt đốt trong nhánh tĩnh mạch giữa của xoang vành -MCV). Tỷ lệ thành công tại các vị trí khác: thành tự do bên trái (97,8%), thành tự do bên phải (93,7%), thành trước bên trái (83,3%) là tương tự các tác giả khác (4,5,8,11).
Bốn trường hợp (2,5%) tái phát trong thời gian theo dõi (3 ở thành tự do thất phải và 1 ở vùng trước vách phải) là do catheter di lệch trong khi cắt đốt. Tỷ lệ này cũng tương tự nghiên cứu của Fred Morady và cộng sự (8). Chúng tôi đã tiến hành cắt đốt lần hai cho 4 trường hợp này thành công và không còn tái phát sau đó khi dùng sheath dài 70 cm để tăng tính ổn định của catheter đốt.
Thời gian thủ thuật:
Thời gian thủ thuật trung bình 93 ± 39 phút, ngắn nhất (30 phút) ở BN có cầu Kent giữa vách phải (không cắt đốt) và dài nhất (240 phút) ở BN có nhiều cầu Kent bên trái, tương tự kết quả của Hugh Calkins và cộng sự. Tác giả này còn khuyên không nên kéo dài thủ thuật quá 3 giờ vì tỷ lệ thành công sau đó rất thấp do thủ thuật viên mệt mỏi và có phù nề quanh vị trí đường dẫn truyền phụ gây nên bởi các nhát đốt trước đó(1,2) .Thời gian chiếu tia X trung bình 16,7 ± 12,3 phút là an toàn cho BN (tỷ lệ sinh ung <0,08%) (9,10) khi so sánh với tỷ lệ đột tử hàng năm ở BN có HC WPW là 0,05 – 0,5% (5).
Các biến chứng
Không có các biến chứng nghiêm trọng đe dọa tính mạng của BN. Chỉ có một BN xuất hiện tụ máu lớn tại chỗ chọc động mạch đùi phải sau thủ thuật cắt đốt đường dẫn truyền phụ vùng sau vách trái. Tỷ lệ này (<1%) cũng tương đương các nghiên cứu khác (6,11). Sau khi băng ép và bất động 24 giờ thì lại bị huyết khối tĩnh mạch chậu đùi bên trái. Bệnh nhân được dùng kháng đông với heparin trọng lượng phân tử thấp gối đầu warfarin và xuất viện sau 1 tuần khi chân trái giảm sưng và đi lại được. Do vậy, dùng Heparin trọng lượng phân tử thấp (Enoxaparin 40mg tiêm dưới da một lần duy nhất sau thủ thuật) có lẽ thích hợp ở tất cả các bệnh nhân cần bất động trên 12 giờ để ngừa huyết khối tĩnh mạch sâu sau thủ thuật.
Các yếu tố dự đoán thủ thuật cắt đốt khó
Đường dẫn truyền phụ ở vùng giữa vách, vùng trước vách phải hoặc thành tự do bên phải, hoặc có tính dẫn truyền từng lúc là những trường hợp chúng tôi gặp thất bại (8 trường hợp, chiếm tỷ lệ 5%). Lý do cắt đốt khó khăn là nguy cơ block nhĩ thất cao (đối với đường dẫn truyền phụ vùng giữa vách và trước vách phải), độ ổn định của catheter cắt đốt không cao (đường dẫn truyền phụ thành tự do bên phải) hoặc khó dò tìm chính xác vị trí (đường dẫn truyền phụ có tính dẫn truyền từng lúc). Tuy số trường hợp này chưa đủ nhiều nhưng cũng phù hợp với y văn (3,4,13).
KẾT LUẬN
Kết quả nghiên cứu một lần nữa chứng minh cắt đốt qua catheter đường dẫn truyền phụ nhĩ thất bằng sóng cao tần có thể được thực hiện an toàn và hiệu quả ở đa số bệnh nhân, không cần phải dùng thuốc điều trị kéo dài. Có thể cân nhắc kỹ thuật này như là một chọn lựa điều trị đầu tay ngay cả cho những BN có điện tâm đồ của hội chứng WPW mà không có triệu chứng hoặc không có bằng chứng cơn nhịp nhanh, nhất là ở những người làm các nghề có tính rủi ro cao như phi công, tài xế, vận động viên (3,7). Tuy nhiên cần cân nhắc giữa nguy cơ-lợi ích khi quyết định cắt đốt cầu Kent vùng trước vách hoặc giữa vách vì nguy cơ block nhĩ thất rất cao.
TÀI LIỆU THAM KHẢO
- Calkins H, Langberg J, Sousa J et al (1992). Radiofrequency catheter ablation of accessory atrioventricular connections in 250 patients. Abbreviated therapeutic approach to Wolff- Parkinson-Whitesyndrome. Circulation, 85:1337-1346.
- Calkins H, Yong P, Miller JM et al (1999). Catheter Ablation of Accessory Pathways, Atrioventricular Nodal Reentrant Tachycardia, and the Atrioventricular Junction : Final Results of a Prospective, Multicenter Clinical Trial. Circulation, 99:262-270.
- Chugh A, Bogun F, Morady F (2008). Catheter ablation of accessory pathways. In Wilber DJ, Packer DL, Stevenson WG. Ablation of Cardiac Arrhythmias, 3rd ed, pp 149-170. Blackwell Futura, Massachusetts.
- Hessling G, Schneider M, Schmitt C (2006). Accessory Pathway. In Schmitt C, Deiselhower I, Zrenner B. Catheter Ablation of cardiac arrhythmias, 1st ed , pp 84-101. Steinkopff Damnstadt, Munich.
- Hogenhuis W, Stevens SK, Wang P, et al (1993). Cost-effectiveness of radiofrequency ablation compared with other strategies in Wolff-Parkinson-White syndrome. Circulation 1993,88 (suppl. II):437-446.
- Jackman WM, Wang X, Friday KJ et al (1991). Catheter ablation of accessory atrioventricular pathways (Wolff-Parkinson-White syndrome) by radiofrequency current. N Engl J Med, 324:1605-1611.
- Klein GJ, Prystowsky EN, Sharma AD, Laupacis A (1989). Asymptomatic Wolff-Parkinson-White syndrome: Should we intervene? Circulation, 80:1902-1905.
- Morady F: Catheter ablation of supraventricular arrhythmias (2004). State of the art. J Cardiovasc Electrophysiol, 15:124–39.
- National Research Council (1990). Recommendations of the International Commission on Radiological Protection. Health Effects of Exposure to Low Levels of Ionizing Radiation. National Academy Press.
- Shapiro J: Radiation Protection (1981). A Guide for Scientists and Physicians. Harvard University Press, pp 324-474. Cambridge, Mass/London.
- Thakur RK, Klein GJ, Yee R (1994): Radiofrequency catheter ablation in patients with Wolff-Parkinson-White syndrome. Can Med Assoc J., 151:771-775.
- Tôn Thất Minh (2004). Khảo sát điện sinh lý và cắt đốt bằng năng lượng sóng có tần số radio qua catheter để điều trị nhịp nhanh trên thất. Luận án Tiến sĩ Y học, Đại học Y Dược TP Hồ Chí Minh.
- Wood MA (2006). Ablation of free wall and posteroseptal accessory pathways. In Huang SKS, Wood MA. Catheter Ablation of cardiac arrhythmias, 2nd ed, pp 371-399. Sauders-Elservier, Philadelphia.












 Xem phản hồi
Xem phản hồi Gửi phản hồi
Gửi phản hồi


